لیشمانیازیس بیماری مشترک انسان وحیوان است که میزبان مخزن بین حیوانات وحشی است.حیوانات اهلی به عنوان دومین میزبان مخزن به شمار می آیند.این انگل بصورت اماستیگوت درمهره داران وبصورت پروماستیگوت درحشرات دیده میشود.
كشف ليشمانيا به عنوان عامل بيماري كالاآزار
سال 1903 ويليام ليشمن و چالز دونو وان اما ستيگوت(1) را درون ماكروفاژهاي افراد مبتلا به كالا آزار مشاهده نمودند.
چرخه حياتي (سيكل زندگي)
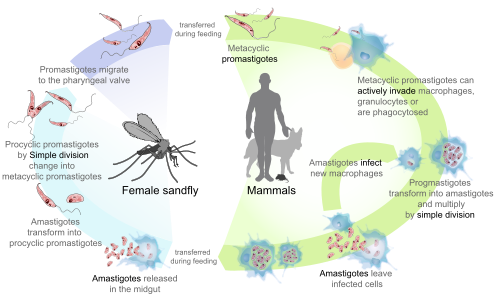
جنس ليشمانيا متعلق به خانواده تريپا نوزوماتيده كه آنهم جزء تك ياخته هاي كينتوپلاستيده(2) است كينتوپلاستيدها متعلق به شاخه او گلنوزوا كه تك ياخته او گلنوئيدهم جزء همين شاخه است . ليشمانيا داراي دو مرحله تكثير است ( Digenetic ) يا چند ميزبانه (Hetero xenous ) است كه بعنوان انگل در حشرات و مهره داران عمل مي كنند ميزبان هاي مهره دار شامل پستانداران و مارمولك هاست ميزبان هاي پستاندار آن انسان ، سگ و بعضي جوندگان است . 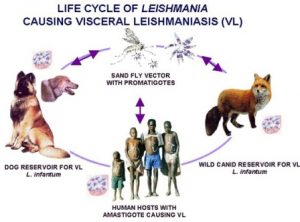
اين انگل ها (ليشمانيا ها ) بيماريهاي پيچيده اي را ايجاد مي كنند كه موسوم به ليشمانيازيس است . گونه هاي ليشمانيايي عهد جديد و عهد قديم شناخته شده اند و در هر دو بيماري مي تواند جلدي يا احشايي باشد . حشره هاي ناقل پشه خاكي از جنس فلوبوتوموس phlebotomus و لوتزوميا ( Lutzomyia ) است كه در آنها انگل بصورت پروماستيگوت در لوله گوارش زندگي مي كنند كه در هنگام خونخواري از بخش پيشين لوله گوارش (foregut ) مسدود شده توسط انگل به زخم وارد میشود.
1- آماستيكوت : مرحله ابتدايي چرخه زندگي در تويپالوزوم كه پيكر مدور و بدون تاژك دارند .
2- كينتوپلاست : جسم ضميمه اي است در ماستيگوفوراها كه داراي DNA است و تكثير مستقل دارد
مرفولوزی
لیشمانیاازنظرشکل بردوگونه است شکل پروماستیگوتی وشکل درون سلولی آماستیگوتی.
مراحل مختلف چرخه حياتي تريپانوزوماتيد .
a- پروماستيگوت
b- آپيستوماستيگوت
c- اپيماستيگوت
d- تریوماستیگوت
e- كوانوماستيگوت
f- آماستيگوت
g- پاراستيگوت
N-هسته
ّ-Fتاژك
K-كينتوپلاست
پروماستيگوت از پشه خاكي ( اندازه 20-14 نانومتر ) توسط ماكروفاژهاي ميزبان هاي پستاندار بلعيده مي شود. و تبديل به آماستيگوت ( به اندازه 4-2 نانومتر ) مي شود انگل در واقع درون فاگوليزوزوم ماكروفاژ زندگي ميكنند آنها تقسيم شده و پس از تركاندن سلول وارد سلولهاي ديگر مي شود در محل ابتدا توليد يك پاپول كوچك مي كند .
انگل ليشمانيا ترو پيكا عهد قديم توليد ليشمانيازيس جلدي مي كند ، اغلب خود به خود بهبود مي يابد و موسوم به زخم شرقي ( سالك ) مي باشد در حاليكه انگل ليشمانيا دونواني بداخل سلول هاي پوشينه اي سيستم تورينه – پوشينه اي و گلبول هاي سفيد با هسته چند شكلي خون ، طحال ، غدد لنفاوي ، مغز استخوان و در نهايت ايجاد ليشمانيازيس احشايي مي كند كه در صورت عدم درمان ممكن است كشنده باشد .
ليشمانيازيس مخاط جلدي عهد جديد ايجاد يك جراحت ( لزيون ) در محل گزش مي كند كه مي تواند ريشه ( متاستاز) به بيني و دهان بدهد و باعث بد ريختي و بيماري غير قابل درماني را بنمايد .
انگل ها بوسيله پشه خاكي در هنگام خونخواري گرفته مي شود و وارد لوله گوارش شده و در بخش مياني لوله گوارش ( Mid gut ) تكثير يافته و تبديل به پروماستيگوت شده به سرعت موجب انسدادلوله گوارش شده و واردمري میشود
جرخه زندگی لیشمانیا در پشه خاکی
اين پروماستيگوت ها مي توانند در 25 درجه سانتيگراد پر ورانده شود. معمولا اماستيگوت ها در داخل سلول ها کشت يافته رشد داده مي شوند اما مي تواند در خارج سلولي در 37 درجه در شرايط خاص رشد داده شود .
بيماريهاي ليشمانيايي
ليشمانيازيس احشايي ( كالا آزار )
بيمار باليني در واقع طيفي از نشانه هاي باليني است كه هم تحت تاثير گونه هاي ليشمانيا و هم واكنش ايمني ميزبان است عفونت ليشمانيا دونوواني با دوره كمون 4-2 ماه از بدون نشانه تا بروز بيماري كامل فرق مي كند .
بيماري باتب و بيقراري شروع شده و با تحليل رفتن ، بزرگي طحال و كبد ادامه يافته و در نهايت پس از 3-2 سال موجب مرگ مي شود در بعضي از موارد كه بيماري بصورت حاد است با تب بالا و لرز و در نهايت در 12-6 ماه موجب مرگ ميگردد .
علت مرگ معمولا در اثر عفونت هاي ثانويه است بعضي از عفونت ها هم خود بخود بهبود ي مي يايند.
اماستيگوت هاي ليشمانيا دونواني در اسمير طحال كه با گيمسا رنگ آميزي و با روغن سدر مشاهده مي شود به هسته و كينتوپلاست ميله اي شكل توجه كنيد ( از T.C- ORITEL 19996 )
اماستيگوت ها در سال 1900 از اسمير طحال سربازي از دام دام ( DUM DUM ) هند توسط ويليام ليشمان كشف شد ( بيماري در هند موسوم با كالاآزار يا تب دام دام است ) ليشمان اين موضوع را در سال 1903 منتشر كرد و همزمان با او چارلز دونوان نيز موفق به كشف اين انگل شد در بعضي از مناطق در 10-5 درصد از موارد درمان شده آشفتگي پوستي ايجاد مي شود كه موسوم به تظاهر ليشمانيايي جلدي پس از كالا آزار است ( PKDL)
ليشمانيازيس جلدي (سالک)
از آنجائيكه تمام ليشمانياها مرفولوژي مجزايي دارند . محققين در ابتدا سه گونه ليشمانيا رامعرفي نمودند تروپيكا (جلدي ) برازيلنيس ( جلدي مخاطي ) و دونوواني ( احشايي ) بهر حال طبقه بندي متداول خيلي پيچيده تر و باز تاب پيچيدگي نشانه هاي است بعنوان مثال انگل هاي كالا آزار هندي و مديترانه ليشمانيا دونوواني و ليشمانيا اينفانتوم
ليشمانيازيس جلدي عهد قديم
دو گونه از ليشمانيا باعث بيماري جلدي در خاور نزديك مي شود . ليشمانيا تروپيكا و ليشمانياماژور بعد از گزش پشه خاكي (فلوبوتوموس ) آلوده ابتدا يك برجستگي جوش مانند ( نودول ) كه ناشي از تجمع سلول هاي پلاسمايي ، لنفوسيت و ماكروفاژهاست بوجود مي آيد .
ليشمانيا ماژور يك بيماري مناطق روستايي و ليشمانيا تروپيكا معمولا در شهرها اتفاق مي افتد در محل جوش زخمي باندازه 3-1 سانتي متر شكل مي گيرد كه اطراف آن آماسي است انگل ها در زخم تكامل يافته پراكنده است مخصوصا در ناحيه حاشيه اي آن بهبودي در عرض چند ماه صورت مي گيرد و ايمني پايدار شكل مي گيرد .
زخم هاي ليشمانيا ماژور ممكن تا حصول بهبودي چند سال طول بكشد زخم هاي ليشمانيا تروپيكا خشك و ليشمانيا ماژور مرطوب هستند هر دو تا ممكن است به عفونت هاي ثانويه آلوده گردند ( yaws ) از جمله ياوز ( يك بيماري پوستي غده غده اي شدن كه ناشي از نوعي اسپيروكت است ) و مياز ( آلودگي زخم بالا رو حشرات ) بعد از بهبود زخم چه بصورت خود بخود و چه درمان يك ايمني پايداري بوجود مي آيد.
ليشمانيازيس جلدي عهد جديد
ليشمانيا عهد جديد به مراتب پيچيده تر مي باشد و در اثر ليشمانيا شاگاسي كه ايجاد بيماري احشايي مي كنند ليشمانيا گروه مكزيكي ( مكزيكان گروپ ) كه ايجاد جراحت خود بهبودي يابنده پوستي مي كند و گروه ليشمانيا برازيلنيسیس كه ايجاد جراحات جلدي و مخاطي – جلدي مي كند بيماري بصورت نقاشي و حك شده بر روي سفال هاي بدست آمده از پرو كه متعلق به 400 سال پيش از ميلاد مسيح است نشاند داده شده است بيماري در تمام كشورهاي آمريكايي لاتين بجز شيلي واروگوئه گسترش دارد و مواردي هم از تگزاس گزارش شده است بيماري يك بيماري مشترك بين انسان و حيوان است كه میزبان مخزن در بين حيوانات وحشي دارد .
جراحت اوليه در انسان بصورت زخمي است كه مركز آن گرد مثل دهانه آتشفشان و اطراف آن التهابي است .
ليشمانيا مكزيكانا ايجاد زخم شيكلروس مي كند كه مي تواند تقريبا باعث تخريب تمام گوش خارجي شود .
ليشمانيا برازيلينسيس ايجاد زخم هاي متاستازي در بيني و مخاط حلق مي كند اين زخم ها ممكن است در عرض چندماه تا چند سال از آغاز عفونت بوجود آيند بيماري عمدتادرافراديكه شاغل در جنگل هستند بروز مي كند و موسوم به اسپانديا مي باشد تخريب جنگل ها موجب گرايش و تطابق بعضي از گونه هاي پشه خاكي در محيط هاي مسكوني و لذا دام اهلي بعنوان دومين ميزبان هاي مخزن بشمار مي آيند .
بيماري اغلب همراه بالاغري مفرط ( كاشكسي ) و به دنبال بهبودي ، آشفتگي ( دفورمیتی ) اعضاء مشاهده مي شود .
اغلب بافت هاي استخواني و غضروفي بيني و همچنين كام سخت و نرم از بين مي روندومرگ بدنبال عفونت ثانويه يا سوء تغذيه رخ مي دهد .
و گاه بيماري به اشتباه جذام و يا ديگر عفونت هاي باكتريايي و قارچي تشخيص داده مي شود
در بعضي از بيماران ، مخصوصا در ونزوئلايك فرم جلدي منتشر از بيماري كه باگرانولوماي ماكروفاژي و ضخيم شدن پوست مشخص شده مشاهده ميشود.اين فرم مثل جذام لپرو ماتوزي و مثل بيماريهاي قارچي است و گاه در تشخيص دچار اشتباه مي كند
پراكندگي ليشمانيازيس
حدود 12 ميليون نفر از 88 كشور جهان به ليشمانيازيس مبتلا ست از كشورها 16 كشور جز كشور هاي توسعه يافته جهان هستند تخمين زده مي شود حدود 350 ميليون نفر در معرض ابتلا به گونه هاي مختلف ليشمانيا هستند .
بروز موارد جديد در سال ، حدود 2 ميليون نفر است ( 5/1 ميليون ليشمانياي جلدي و نیم میلیون نفر ليشمانياي احشايي) مثل خيلي از بيماريهاي گرمسيري عفونت هاي ليشمانيايي با توسعه اقتصادي ساخت بشر و تغييرات محيط اطراف توسط انسانها باعث افزايش تعارض ( در معرض قرار گرفتن ) انسان با پشه خاكي ناقل بيماري باشد برداشت الوار از جنگل ها استخراج معادن ، سدسازي ها ، تعريض اراضي براي كشت ، برنامه هاي جديد آبياري ، جاده سازي و جنگل ها دست نخورده از جمله در آمازون ، گسترش مهاجرت هاي اقتصادي و شهرنشيني هاي فزاينده و سريع در سطح جهان علل اصلي افزايش موارد ابتلا به اين بيماري است .
بيماري هميشه بعنوان يك زئونوز بوده است . نوعي از موش موسوم به جربيل بعنوان اصلي ترين مخزن ليشمانيا تروپيكا در مركز آسياست و در بعضي از مناطق سگ وگربه وسنجاب ها نيزعفوني ميگردند . در آمريكاي لاتين جوندگان بعنوان مخزن براي گونه هايي از ليشمانيا هستند .
اخیرا یک افزایش درلیشمانیای احشائی پدیدآمده که ناشی ازاشاعه جهانی ایدز میباشدعفونت توامان ایدز لیشمانیا رامیتوان یک بیماری وابسته یاگرایشی واقعی بحساب آوردمخصوصادراروپای جنوبی که70-25 درصدازلیشمانیای احشائی بالغین وابسته به عفونتHIV بوده است9-5/1درصداز مواردایدزازبیماری لیشمانیای احشائی تازه گرفتار شده ویادوباره فعال شده رنج می برندهمه گیری هائی از لیشمانیا احشائی هنوز هم درسودان شرقی و جنوبی ودرتقاطع اریتره اتیوپی وسودان بروز می کند اخیرا بروز مجددی از لیشمانیای احشائی در برزیل رخ داده است.
شرح ذيل نقشه پراكندگي جهاني تيپ هاي مختلف ليشمانيا از وب سايت Oppedaes است
شيوع ليشمانيازيس در سگ هاي شكاري ايالات متحدي
در سال 1999 سگ هاي شكاري باشگاهي در ميل بروك نيويورك مبتلا به يك بيماري ناشناخته اي شدند نشانه هايي كه در آنها مشهود بود عبارت بودند از ضعف , خونريزي , از دست دادن موها و نارسايي كليه , بيش از 24 تا از سگ ها مردند . آزمايش مايعات مفصلي سگ هاي بيمار منجر به شناسايي انگل هاي ليشمانيايي شد و پس از آن تمام سگ هاي شكاري ( Fox hound ) آمريكا تحت آزمايش قرار گرفتند و 12 درصد از آنها پادتن بر عليه ليشمانيا داشتند ولي نه در سگهاي ولگرد ميل بروك و نه سگهاي ولگرد ساير نقاط آمريكا پادتني مشاهده نشد
.انتقال اين بيماري مبهم بود .چون از چهارگونه پشه خاكي موجود در ايالات متحده هيچكدام به جز در نیوجرسي قادر به زندگي در شمال نيستند . دانشمندي در والتر رايد چنين نظريه داد كه سگها با تماسهاي جنسي يا تماس زخمها ممكن است همديگر را آلوده كرده باشند البته متخصصين ليشمانيا با اين نظر موافق نيستند .
آنها نظرشان براين است كه سگها زمانيكه در سفر جنوب بودند بوسيله پشه خاكي گزيده شده اند يك احتمال ديگر اينكه گونه ناشناخته اي از پشه خاكي در محل باشد يا حتي ناقلين ديگري وجود داشته باشد گونه ليشمانيا , ليشمانيا ايفانتوم است كه به احتمال پايين بودن سطح اپيدميكي آن در افراد ايالات متحده وجودش فراموش شده است .
تشخيص و درمان ليشمانيازيس
تشخيص بيماريهاي ليشمانيايي منحصراًبا شناسايي اماستيسگوت در كشت انگلي و يا روش ميكروسكوپي ا ست اخيراً PCR ژن هاي انگلي جهت تشخيص مورد استفاده قرار مي گيرد .
بيوسپي بافتي را به صافي هاي مخصوص تماس داده و سپس صافي ها را با الگوهاي معلوم در مقابل ژن هاي انگل روبرو ميكنند . درمان بيماريهاي ليشمانيايي هم بصورت موضعي و هم بصورت عمومي با استفاده از تركيبات پنج ظرفيتي آنتيموان و تركيبات معطره دياميدين انجام ميگيرد رايج ترين تركيبات مورد استفاده از آنتيموان پنج ظرفيتي استيبو گلوكنات سديم ( پنتوستام ) در آنتي مونيات ملگوسين (گلوكانتيم) كه براي اولين با در سال 1947 و 1950 بكار گرفته شده است عدم توفيق در درمان و عود بيماري در تمام فرمهاي ليشمانيازيس حدود 25-10 درصد موارد ميباشد اگر اين داروها موثر نبودند از پنتاميدين (لوميدين) و آمفوتريسين B(فانژيزون) كه در سالهاي 1940 و 1959 معرفي شده اند استفاده مي شود .درمان ليشمانياي مخاطي – جلدي موفقيت آميز نيست .
نظر به اينكه آماستيسگوت در درون فاگوليزوزوم ماكروفاژهاي ميزبان قرار مي گيرند لذا واكنش ايمني هومورال بدليل مخفي بودن انگل ليشمانيا شكل نمي گيرد از آنجائيكه انگل هاي درون سلولي در معرض واكنش هومورال ميزباني نيستند پادتن هاي گردش خون تاثيري بر عفونت ندارند وحتي ممكن است مضر نيز واقع شوند ايمني بطور كلي وابسته به ایمنی سلول است و اين براساس مشاهدات زير است .
1- تخليه سلولهاي Bدر حيوانات تاثيري بر جريان يك عفونت ندارد .
2- جلوگيري از عمل پادتن ها بوسيله ضد(m (Igتاثيري بر عفونت ندارد .
3- درحاليكه سطحm Ig و IgG بالاست ولي قادر به حفاظت در برابر عفونت نيست با استفاده از سويه هاي همخون موش هايي كه از نظر ژنتيكي مشخص ومعلوم هستند آنهايي كه در مقابل ليشمانياي ماژور جلدي بهبودي يافتند و آنهايي كه بهبودي نيافتند موجب افزايش دانش ما در مورد واكنش ايمني در برابر ليشمانيا است . دو كشف اساسي در اين سیستم عبارتند از :
1- دو مسير براي سلولهاي كمكي تي ( T Helper ) وجود دارد .افزايش (1 T Helper ) منجر به محافظت و افزايش ( T Helper2 ) منجر به وخامت بيماري ميشود .
2- علاوه بر اين حفاظت خودكار , ماكروفاژها نيز يك سيستم دفاعي ديگر دارند كه با توليد عامل نكروز توموري آنها (TNFalpha) كه باعث تحريك در توليد آنزيم اكسيد نيتريك سنستتاز مي شود .
هرگونه نقص ژنتيكي كليدي در اين مسير خود را مستعد ابتلا به بيماري خواهد نمود استعداد ابتلا به عفونت در موش هاي همخون حداقل بوسيله پنج جايگاه ژن كنترل مي شود .
اين پنج جايگاه ژن عبارتند از SCL-1 , SCL-2 , خوشه ژني سيستوكين T-Helper 2 كمپلكس اصلي بافت رقابتي و NraMp1 يا L Sh مشابه همين براي ژنهاي مستعد كننده انسان نيز شناسايي شده است اين ژن ها همچنين كنترل مقاومت ديگر پاتوژنهاي درون سلولي مثل توكسوپلاسما , سل و جذام را بعهده دارند.
فرعيات Tcell كه Th1 باعث فعال شدن ايمني وابسته سلولي و از واكنش هومورال جلوگیری میکند. درحاليكه سلولهاي Th2 باعث فعال شدن ایمنی هومورال و از ايمني وابسته سلولي جلوگيري ميكند .
واكسنهاي تجربي از سلولهاي كشته شده يا سويه هاي تخفيف حدت يافته در چند منطقه آزمايش شده است . در برزيل ( ليشمانيا امازونيسيس ) و در ونزوئلا ( ليشمانيا مكزيكن و ليشمانيا برازيلنسیس ) به ارتش اشغالگر اسرائيل نيز توصيه شده است كه سربازانشان برعليه ليشمانيا واكسينه كنند علاوه بر اين بعضي از واكسنهاي مولكولي ( واكسن هاي افتراقي ) كه براي آزمايش انتخاب شده اند : GP63 كه مهمترين گليكوپروتئين سطحي ليشمانيا و LPG ( ليپو فسفو گليكان ) سطحي پارازيت است .
واكسن هاي DNA كه تجلي gp63 را دارد معلومشده است تا حدودي موثر است .
· عفونت زايي ليشمانيا هاي پروماتيسگوتي كشت داده شد
آزمايشگاه ديويد ساكس فاش ساخت كه پروماتيسگوت در ناقل پشه خاكي دستخوش تغييرات ظاهري وبيوشيميائي مي شوند بطوريكه عفونت زايي آنها براي ميزبانان پستاندار افزايش پيدا ميكند , آنها توانستند اين فرايند را در كشت انگل تقليد كند .
بطوريكه مرحله Log ( فاز لگاريتم ) غيرعفوني و مرحله خاموشي يا تثبيت عفوني بوده است .آنها اين مراحل را به ترتيب پيش چرخه اي (Procyolic ) و فوق چرخه اي ( Metacyolic ) پروماستيگوت ناميدند .
پروماستيگوت هاي متاسيكلي ليشمانيا ماژور را مي توان با عدم توانايي آگلوتينه كردن لكتين , آگلوتيمين بادام زميني تشخيص داد .
شكلهايي از يك مقاله مربوط به تغييرات كربوئيدرات بين پروماستيگوتهاي ليشمانياي ماژور عفوني و غيرعفوني .دو گالاكتوز متصل به لكتين و آگلوتينين بادام زميني ( PNA ) و آگلوتنين كرچك (RCA ) مي توانند 100% پروماتيسگوت هاي فاز Log را آگلوتينه نماينددر حالیکه فقط 50 در صد پروماستیگوت هامرحله تثبیت راآگلوتینه می کنند افزودن mMD 10گالاكتوز مانع از آگلوكتيناسيون ميشود